Estudios y Ensayos Clínicos
Los registros nos facilitan la realización de Estudios Clínicos Observacionales. Los estudios observacionales no son intervencionistas, es decir, no definen o imponen una estrategia o tratamiento. Nos permiten conocer lo que está pasando en un determinado grupo de pacientes. Son de muy diverso tipo. En algunos solo conlleva el análisis de datos generados en práctica clínica habitual, sobre todo en estudios retrospectivos, es decir, analizando datos previos hasta el inicio del estudio. En otros, se puede añadir la realización de alguna analítica o exploración que añada más información, esto suele ocurrir en estudios de tipo prospectivos, es decir los que se programa su realización a partir de los datos que se obtendrán tras el inicio del estudio en progresivas revisiones.
Existen estudios clínicos prospectivos que se realizan en diferentes centros de un país o de diferentes países ( multicéntricos), en general de alto interés, en el que por ejemplo se buscan factores de la dieta o de la microbiota en la evolución de la Enfermedad Inflamatoria Intestinal (EII), o en las que se vigila la evolución de los embarazos en pacientes con EII.
Es el nivel de investigación más complejo. Es imprescindible para el avance de nuevos tratamientos y estrategias. En estos se han de comparar de forma ‘ciega’ (sin conocimiento del participante ni del investigador) el tratamiento que se quiere investigar, con otro tratamiento o con placebo (una pastilla o bolsa de infusión similar a la del tratamiento ensayado, pero sin efecto farmacológico).
Funcionan dentro de un marco regulatorio estricto con muchos mecanismos para asegurar la seguridad de los participantes. Existen diversas fases en las que un nuevo fármaco debe demostrar ausencia de efectos adversos significativos y eficacia para una enfermedad.
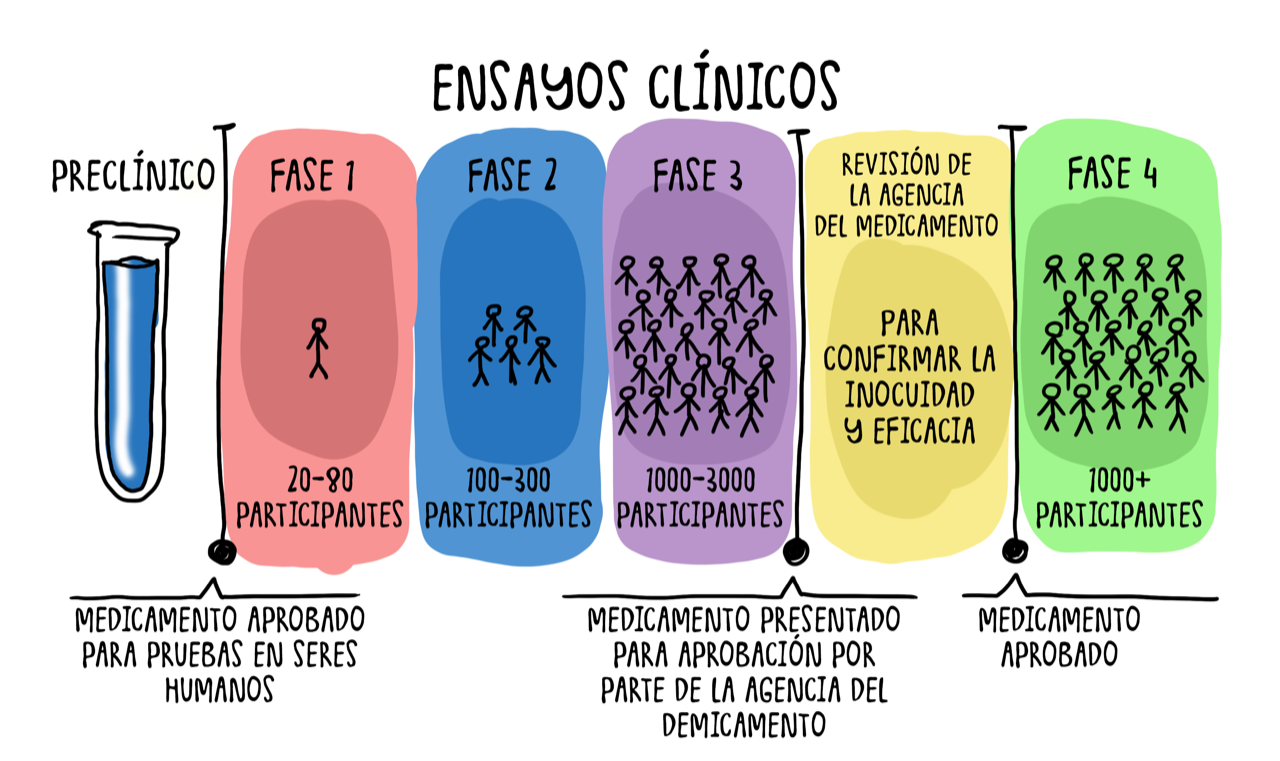
Inicialmente (Fase I), los estudios son básicos (en laboratorio) y con animales de investigación (bajo una regulación). Si se pasa esa fase, los ensayos se realizan en humanos, inicialmente sanos (se valora la seguridad) y posteriormente en pequeños grupos de pacientes (estudios en Fase II). Si se demuestra cierto efecto, se deben realizar estudios en Fase III, que amplían el número de pacientes tratados para confirmar los hallazgos previos. En esta fase generalmente, se juntan un gran número de pacientes de muchos centros a nivel internacional (multicéntrico). En muchos hospitales de nivel terciario en España se colabora en estos estudios en Fase III de distintos fármacos. Si en esta Fase III un fármaco se demuestra eficaz y seguro, conseguirá la aprobación formal para formar parte del arsenal terapéutico por las agencias del medicamento (Agencia EuropeaEMA, Agencia Americana-FDA).
- Fármaco no aprobado: La objeción que puede existir es que estamos recibiendo un tratamiento aún no aprobado. Sin embargo, en Fase III, el tratamiento ensayado ya ha demostrado en Fase II una eficacia y seguridad inicial, con lo que se tiene cierta garantía. Los mecanismos de seguridad y control permiten que si existe un problema se detecte rápido y se actúe en consecuencia.
- Placebo: Por otro lado, puede que al participante se le asigne al grupo placebo que no recibe el tratamiento. En muchos casos la probabilidad de asignación al fármaco ensayado es mayor a la de recibir placebo (a veces 2/1 o 3/1). Además, existe un grupo de pacientes que responden al placebo en todos los ensayos clínicos que suele estar entre un 15-25% (el denominado ‘efecto placebo’). Aún así si existe empeoramiento de la enfermedad va a existir un mecanismo para poder rescatar al paciente, con opción de recibir en segunda opción el tratamiento ensayado, de aumentar el tratamiento convencional o en cualquier momento salir del estudio. Se primará siempre la seguridad del paciente.
- Aumento de visitas y exploraciones: En los ensayos clínicos, dada su naturaleza, existe un gran control del paciente. Las visitas son frecuentes, y se realizan analíticas y pruebas complementarias repetidas, pero son la forma que permite objetivar la respuesta al tratamiento.
- Fármaco nuevo: Muchas veces se espera del fármaco en desarrollo un beneficio respecto a los fármacos que ya se usan habitualmente para esa dolencia. Pueden aportar mayor eficacia, mayor efecto a largo plazo o mayor seguridad. Incluso en grupo placebo, si no tiene respuesta, existe muchas veces un mecanismo de tratamiento ‘en abierto’, lo que quiere decir que tiene oportunidad igualmente de recibir el tratamiento ensayado.
- Mayor control: Al participar en un ensayo clínico, los pacientes de forma automática van a estar más controlados en la evolución de la enfermedad, no solo por las visitas, sino además manteniendo un contacto cercano con el equipo investigador, ya que cualquier incidencia se recoge.

- Conocimiento sobre la enfermedad: Los ensayos clínicos aportan un avance en el conocimiento de la enfermedad, su manejo y tratamiento. Es la manera más fiable de demostrar la eficacia de nuevos tratamientos. Estos se sumarán en el futuro al arsenal terapéutico. El objetivo es descubrir tratamientos eficaces, seguros y que mantengan su efectividad a largo plazo. Seguramente cada paciente necesite un tratamiento específico y conocer marcadores de respuesta a cada uno de ellos es otro gran objetivo.
Desde aquí damos las gracias a la generosidad de los pacientes y a al esfuerzo de los equipos investigadores.
Gracias!!!!


