Virus del papiloma humano
Información realizada y revisada por Dra. Marta Calvo Unidad EII. Hospital Puerta de Hierro. Madrid; Dra. Raquel Abelleira Sanjurjo y Dra. María Aurea Calaza Vázquez. Ginecología. Complejo Hospitalario Universitario de Ferrol; Dra. Covadonga Castro. Ginecología. Complejo Hospitalario Santiago de Compostela.
- 1. ¿Qué es el virus del papiloma humano?
- 2. Si tengo infección por el VPH, ¿puedo desarrollar cáncer de cuello de útero?
- 3. ¿Cómo puedo prevenir el cáncer de cuello de útero?
- 4. ¿Cómo me pueden diagnosticar el cáncer de cuello de útero?
- 5. ¿Cómo me pueden tratar el cáncer de cuello de útero
- 6. ¿Existen vacunas eficaces frente al VPH?
- 7. ¿Cuándo debería vacunarme del VPH?
1. ¿Qué es el virus del papiloma humano?
Uno de los descubrimientos más importantes en la investigación del cáncer de los últimos 30 años, ha sido la demostración de que el cáncer de cuello uterino de útero (cérvix) está causado por el virus del papiloma humano (VPH), un virus de transmisión primordialmente sexual.
Este cáncer lo podemos considerar como la secuela a largo plazo de una infección no resuelta por ciertos tipos de VPH. La familia de los VPH cuenta con más de 150 tipos virales que en relación con su capacidad para desarrollar el cáncer, se clasifican en tipos de alto y de bajo riesgo de producir cáncer.
La infección persistente, o no resuelta, por VPH de alto riesgo es responsable del 99,8% de los cánceres de cuello de útero; así como de otros tipos de cáncer de vagina, vulva, ano, pene, cavidad oral y orofaringe. Ejemplos de VPH de alto riesgo lo constituyen los VPH de tipo 16 y 18, responsables, a escala mundial, del 70% de los cánceres de cuello de útero y de los de bajo riesgo los VPH de tipo 6 y 11. Estos últimos rara vez se encuentran en lesiones cancerígenas y son los responsables del 90 % de las verrugas genitales, también llamadas condilomas acuminados.
El VPH puede considerarse, después del tabaco, el segundo carcinógeno (agente físico, químico o biológico con capacidad potencial de producir cáncer) en humanos, pues se estima que a nivel mundial está asociado a un 5% de todos los cánceres en humanos y a un 10% de los cánceres en la mujer.
2. Si tengo infección por el VPH, ¿puedo desarrollar cáncer de cuello de útero?
La infección genital por el VPH es la infección de transmisión sexual más frecuente.
En menores de 25 años puede llegar a afectar al 70% de la población. No produce síntomas y en la mayor parte de los casos se cura espontáneamente. La pareja sexual puede ser portadora de la infección, aunque no presente síntomas; no siendo necesario el uso de ninguna prueba diagnóstica para confirmar la infección, la cual generalmente se curará de manera espontánea.
Es importante saber que la infección por el VPH de alto riesgo (VPH-AR) es la causa necesaria pero no suficiente para llegar al cáncer de cuello. De las mujeres infectadas, la gran mayoría nunca presentarán cáncer, esto se debe a que han de existir otros factores que modulen el paso de la infección a la transformación tumoral, de todos los que existen, el más importante y reconocido cofactor es el tabaco.
El VPH de alto riesgo o con capacidad de producir cáncer hace que la célula infectada tenga menos capacidad de controlar su ciclo celular y de poder repararse de la forma en lo que lo haría habitualmente, esto supone un proceso largo de transformación por el que las células evolucionan desde la normalidad a adquirir cambios premalignos y finalmente a cáncer invasor.
Las lesiones premalignas se denominan displasias o neoplasias cervicales intraepiteliales (CIN), de las que existen 3 grados: Displasia leve o CIN 1, Displasia moderada o CIN 2 y Displasia severa o CIN3.
Los pacientes con EII en tratamiento con fármacos inmunosupresores, especialmente tiopurinas (azatioprina, mercaptopurina), presentan una mayor incidencia de infecciones por VPH especialmente los relacionados con la aparición de verrugas cutáneas y una peor evolución de las mismas en comparación con los pacientes sin tratamiento inmunosupresor. Existe algún trabajo que describe la aparición o empeoramiento de condilomas genitales en pacientes en tratamiento con anticuerpos anti-factor de necrosis tumoral (TNF) como infliximab.
En el momento actual, todavía existe controversia en los trabajos publicados sobre si las pacientes con EII presentan un mayor riesgo de infección VPH y de cáncer de cuello de útero que la población general. Algunos estudios publicados refieren una mayor incidencia de citologías cervicales anormales y lesiones de mayor grado en pacientes con EII cuando se comparan con mujeres sanas, si bien pueden existir factores de confusión como el tabaco o el riesgo sexual, que no se tienen en cuenta en todos ellos. Asimismo, se ha descrito que el uso de inmunosupresores aumenta el riesgo de presentar una citología anómala a partir de los 6 meses de tratamiento.
Dra. Covadonga Castro – Servicio de Ginecología del C.H.U. de Santiago de Compostela.
3. ¿Cómo puedo prevenir el cáncer de cuello de útero?
La sensibilidad de la citología no es del 100%, eso significa que no puede detectar todas las lesiones que existen, de ahí la necesidad de repetición anual o trianual (cada 1 o 3 años). Si estás inmunodeprimida, como en el caso de tomes tratamiento inmunomodulador, el intervalo ha de ser anual.
Puedes disminuir el riesgo de desarrollar cáncer de cuello de útero o facilitar su curación, tomando las siguientes medidas:
- Preservativo: El preservativo usado correctamente en todo momento de la relación sexual no sólo será eficaz para evitar y/o disminuir la infección, sino que una vez que la mujer tiene una displasia y es tratada, ayudará en la curación.
- Tabaco: Si tienes displasia, deberías dejar de fumar.
- Anticonceptivos hormonales: El caso concreto de cada paciente será valorado en la consulta, no obstante, si los tomas desde hace más de 10 años, se recomienda suspenderlos.
- Vacunación del VPH: Es importante seguir las recomendaciones de vacunación contra el VPH que te indique el médico o especialista.
4. ¿Cómo me pueden diagnosticar el cáncer de cuello de útero?
Ante el resultado de una citología anormal debe establecerse siempre que sea posible un diagnóstico de confirmación. Cuando la mujer con un estado de inmunodepresión presenta una citología alterada con una lesión intraepitelial no se repite la citología, como podría ser adecuado en otros casos, sino que se remite a consultas de Ginecología para realizar una colposcopia y tomar una biopsia de las lesiones sospechosas.
Sala de colposcopias y material empleado en la realización de la colposcopia
La colposcopia es una técnica basada en la exploración aumentada de los epitelios (tejidos) del cuello uterino, la vagina y la vulva. El instrumento que se utiliza, se llama colposcopio, y consta básicamente de una lupa, que facilita el enfoque y una fuente luminosa potente. Con él conseguimos visualizar el cuello del útero con diferentes aumentos, después de haberlo teñido con dos tinciones diferentes. La colposcopia no permite conocer las características histológicas de los tejidos, es decir, analizarlos, pero sí localiza la lesión y delimita su extensión permitiendo guiar al colposcopista al lugar adecuado y preciso, para realizar la biopsia. La técnica no requiere ningún tipo de preparación ni anestesia, ya que resulta indolora.
Durante el embarazo se realizará de igual forma, sin emplear lugol (solución compuesta por yodo y cloruro potásico, disueltos en agua destilada). En este caso, si precisa una biopsia, el cuello sangra con más facilidad, pero la embarazada ha de saber que esto no supone un riesgo para su gestación.
5. ¿Cómo me pueden tratar el cáncer de cuello de útero
El tratamiento deberá ser individualizado en cada mujer, ya que el mismo resultado de la biopsia en unas pacientes sólo requerirá control periódico, y en otras puede precisar un tratamiento especifico.
Existen dos tipos de tratamientos:
- Tratamientos destructivos locales:
a. Criocoagulación: consiste en la destrucción del tejido con frío, se utiliza en lesiones pequeñas y de bajo grado.
b. Vaporización láser: la destrucción del tejido se consigue mediante un haz de luz de elevada densidad de energía. Es una alternativa cara y que no tienen en todos los hospitales.
- Tratamiento escisional o cirugía: La Conización del cuello del útero, suele ser el tratamiento de elección. Consiste en quitar en el quirófano un fragmento del cuello del útero (cono cervical) que posteriormente se envía al Servicio de Anatomía Patológica, para su análisis. Es un procedimiento de corta duración, que habitualmente, no requiere ingreso hospitalario, y que como único cuidado posterior requiere que la paciente no mantenga relaciones sexuales, ni utilice tampones vaginales hasta la exploración de control, que se realizará en la consulta en el plazo aproximado de un mes.
Durante el embarazo será excepcional realizar una conización salvo que exista una alta sospecha de cáncer en la biopsia, en cuyo caso estaría indicada su realización. En los demás casos, la paciente embarazada se controlará de nuevo a las seis semanas del postparto, y si la lesión no ha desaparecido, se hará una conización
6. ¿Existen vacunas eficaces frente al VPH?
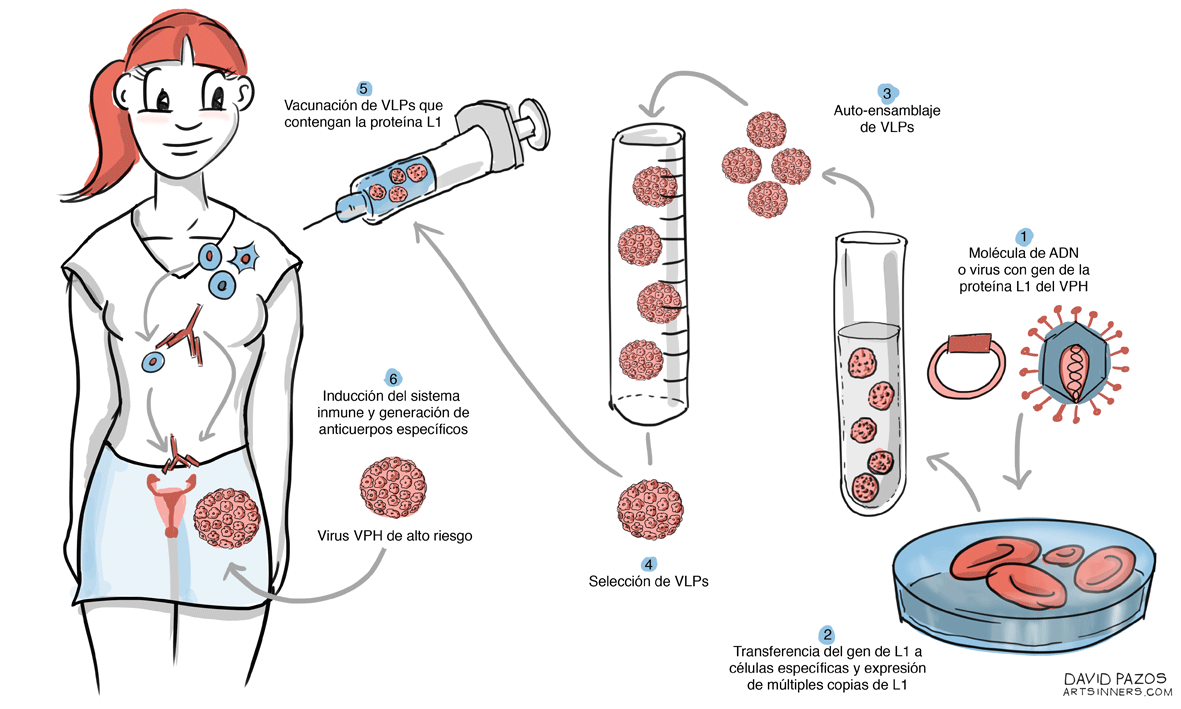
Las vacunas profilácticas o preventivas frente al VPHestán elaboradas mediante una técnica de laboratorio (recombinación genética) que permite la creación de unas partículas similares a los virus que se denominan VLP (Virus Like Particles), parecidos en estructura y composición a las del virus VPH original, pero con la característica de que han perdido su capacidad de infectar a otras células (no poseen el material genético necesario para dicho proceso). Sin embargo, estas VLPs siguen siendo capaces de activar a las células del sistema inmunológico y desencadenar la formación de anticuerpos específicos contra ellas (inmunogenicidad), que ayudan a neutralizarlos y a evitar la futura infección con el VPH. De ahí que la vacunación frente al VPH sea una de las medidas preventivas de primer orden.
El objetivo a largo plazo de la vacunación frente al VPH, es la prevención del cáncer invasor de cuello de útero; mientras que el objetivo a medio plazo es prevenir las lesiones precursoras, especialmente el CIN3.
Actualmente hay diferentes vacunas preventivas disponibles frente al VPH con protección sobre un número diferente de tipos de virus (2, 4 o 9 tipos de virus):
- Cervarix: Vacuna bivalente frente al VPH 16 y 18 implicados en el 70% de los cánceres de cervix.
- Gardasil: Actualmente existen dos tipos de vacunas:
- a. Vacuna tetravalente, protege frente al VPH 16 y 18 de alto riesgo oncogénico (los implicados en el 70% de los cánceres de cuello de útero) y además frente al VPH 6 y 11, que producen las verrugas genitales.
- b. Vacuna nonavalente, frente al VPH 6 y 11 de bajo riesgo oncogénico, con protección frente a verrugas genitales y frente al VPH 16, 18, 31, 33, 45, 52 y 58 de alto riesgo oncogénico, implicados en aproximadamente el 90% de los casos de cáncer de cuello de útero y aproximadamente del 80% de las lesiones de cuello de útero de alto grado (lesiones precancerosas de cérvix, tipo CIN2, CIN3 y adenocarcinoma in situ).
Estas vacunas profilácticas frente al VPH, son vacunas para prevenir el cáncer, pero lógicamente no se puede esperar a la aparición del cáncer para ver si son o no eficaces, por ello se tienen en cuenta otros aspectos relacionados con la infección por VPH (variables intermedias), que permiten confirmar el nivel de protección de la vacuna.
Una de estas variables a controlar y que ha sido propuesta por la OMS como la variable principal, es la capacidad de la vacuna de impedir la infección persistente por VPH; mientras que las variables o aspectos clínicos a controlar es la capacidad de la vacuna de prevenir las lesiones precursoras, el CIN2 y CIN3.
Se ha demostrado que la eficacia de la vacuna frente al VPH se encuentra en el rango del 95,7% y el 100%. A pesar de esta elevada eficacia, el cribado de cáncer de cuello de útero en la población femenina sigue siendo muy importante, por lo que debe mantenerse en poblaciones vacunadas, ya que la vacuna protege del 70% de los posibles cánceres de cuello; además, la vacuna frente al VPH posee protección cruzada (protección adicional que presenta una vacuna frente a otros tipos de virus diferentes para los que no está diseñada específicamente) demostrada frente a ciertos tipos de VPH, por lo que se considera que su eficacia será mayor.
7. ¿Cuándo debería vacunarme del VPH?
Las INDICACIONES de vacunación frente al VPH son las siguientes (Calendario de vacunación):
1. Grupo de máxima prioridad: Mujeres de 9 a 14 años.
Al tratarse de una vacuna preventiva y sin efectos terapéuticos, el momento óptimo de vacunación es antes del inicio de la actividad sexual; ya que la infección por VPH acontece con rapidez tras el inicio de la actividad sexual. Además, la exposición precoz al VPH incrementa el riesgo de infección persistente y de desarrollar lesiones premalignas y cáncer de cuello de útero.
2. Grupo de alta prioridad: Mujeres hasta los 25-26 años.
Se ha demostrado la seguridad, la inmunogenicidad y la eficacia de las vacunas VPH, hasta los 25-26 años; incluso en aquellas mujeres que han estado anteriormente expuestas al VPH, que sólo excepcionalmente habrán estado expuestas a todos los tipos de VPH frente a los que protege la vacuna.
No está indicado hacer determinación de VPH previo a la vacunación. Reduce la reinfección o reactivación de una infección latente, y además potencialmente podría reducir la transmisión viral.
La realización de una vacunación de rescate (pauta acelerada de vacunación) no sólo aporta los beneficios individuales de quienes se vacunan sino que acortan el tiempo requerido hasta la obtención de los beneficios en salud pública y puede mejorar la eficiencia de la vacunación.
El límite de la edad superior de la vacunación de rescate aplicados desde los programas de vacunación pública varía según los países, desde los 16 años de Noruega 18 de Reino Unido o Luxemburgo, hasta los 26 años en Estados Unidos o Australia.
3. Vacunación en pacientes con displasia cervical o tras conización cervical para prevenir la recidiva:
Aunque exista una infección documentada previa por el VPH y/o una displasia cervical, la administración de la vacuna, protege de la infección de las otras variantes del virus incluidas en la vacuna. Por tanto, la presencia de una lesión cervical provocada por el VPH, no supone una contraindicación para la vacuna; aunque la eficacia de la misma pueda ser menor.
Un estudio publicado en Gynecologic Oncology en 2013 muestra que la vacuna reduce las recidivas en pacientes tras conización (se estudió un grupo de 735 pacientes entre 20 y 45 años con displasia de alto grado, presentaron recidiva el 2,5% de las pacientes vacunadas frente al 7,2% en el grupo no vacunado). La falta de vacunación tras la cirugía es, por tanto, un factor de riesgo independiente para la recidiva, multiplicando por 2,84 el riesgo de que ésta se presente.
Respecto a las mujeres con EII, las RECOMENDACIONES actuales de vacunación frente al VPH serían (Calendario de vacunación ):
- Se recomienda la vacunación frente a VPH en mujeres afectas de EII hasta los 26 años (vacuna financiada en mujeres nacidas a partir de 1994 o con factores de riesgo).
- Las pacientes de 26 años o más pueden beneficiarse de la vacunación frente VPH
Está indicado el uso de cualquiera de las vacunas disponibles.
La vacunación puede administrarse en cualquier momento, aunque preferentemente debe administrarse en el momento del diagnóstico, previo al uso de tratamientos inmunosupresores o biológicos, para garantizar una mayor inmunogenicidad (protección frente a la infección mediante la formación de anticuerpos).
La PAUTA de vacunación recomendada depende del tipo de vacuna, de la edad y del estado inmunitario. De forma genérica, las vacunas frente al VPH se administran por vía intramuscular en el deltoides.
- Para la vacuna bivalente (Cervarix®) la pauta de vacunación en adolescentes de 9 a 14 años incluye dos dosis, la segunda administrada a los 6 meses de la primera (flexible entre 5 y 13 meses). La pauta de vacunación a partir de los 15 años de edad es de 3 dosis en los meses 0, 1 y 6.
- Para la vacuna tetravalente (Gardasil®) la pauta de vacunación entre los 9 y los 13 años es también de dos dosis, administradas en los meses 0 y 6. La pauta de vacunación posteriormente es de tres dosis (0,2 y 6 meses).
- Para la nonavalente (Gardasil 9®) el intervalo de edad es de 9 a 14 años. La pauta de vacunación posteriormente es de 3 dosis (0, 2 y 6 meses).
Estas vacunas no están indicadas en menores de 9 años por la falta de estudios sobre inmunogenicidad y seguridad.
En personas con inmunodepresión se recomienda usar siempre la pauta de 3 dosis, independientemente de la edad.
En ningún caso, hasta el momento, está establecida la necesidad de administrar dosis de recuerdo.
Tampoco existen datos por el momento, que permitan recomendar esta vacuna en varones afectos de EII.
La vacunación no está recomendada durante el embarazo, dado que los datos de seguridad son limitados. Si una mujer queda embarazada después de iniciar la pauta de vacunación, se recomienda retrasar las dosis restantes hasta después del parto. Sin embargo, no es necesario tomar ninguna medida en caso de que alguna dosis se administre por error a una mujer embarazada, ya que la vacuna no se ha asociado a efectos adversos en el embarazo o teratogénicos en gestantes que han recibido la vacuna.
Dado que las vacunas actuales no ofrecen cobertura para todos los tipos de VPH oncogénicos, es importante recomendar a todas las mujeres vacunadas que deben seguir las pautas establecidas de cribado de cáncer de cérvix.
El único estudio publicado de eficacia y seguridad de la vacuna del VPH en pacientes con EII demostró una adecuada inmunogenicidad y seguridad de la vacuna tetravalente. La vacuna indujo la aparición de títulos similares de anticuerpos en las pacientes con EII que en los controles sanos, a pesar de que el 49% de los pacientes con EII recibían inmunosupresores y el 51% restante recibían tratamiento con anticuerpos anti-TNF . Por tanto, a pesar de que la evidencia es escasa y en algunos casos contradictoria, todas las guías clínicas de prevención de enfermedades oportunistas en pacientes con EII recomiendan controles clínicos periódicos estrictos y la administración de la vacuna del VPH a las pacientes según las guías nacionales, especialmente si van a recibir tratamiento inmunosupresor.